Pressmitteilung: Der Nobelpreis in Chemie 1995
English
Swedish
German

Die Königlich Schwedische Akademie der Wissenschaften hat beschlossen, den Nobelpreis in Chemie für das Jahr 1995 an
Professor Paul Crutzen, Max-Planck-Institut für Chemie, Mainz, Deutschland (niederländischer Staatsangehöriger),
Professor Mario Molina, Department of Earth, Atmospheric and Planetary Sciences und Department of Chemistry, MIT, Cambridge, MA, USA und
Professor F. Sherwood Rowland, Department of Chemistry, University of California, Irvine, USA
wegen ihrer Arbeiten zur Chemie der Atmosphäre, insbesondere über Bildung und Abbau von Ozon zu verleihen.
Die Ozonschicht – die Achillesferse der Biosphäre
Die Erdatmosphäre enthält kleine Mengen von Ozon – ein Gas, dessen Moleküle aus drei Sauerstoffatomen (O3) bestehen. Würde man das gesamte Ozon der Erdatmosphäre in eine Schicht bei dem an der Erdoberfläche existierenden Normaldruck zusammenpressen, so würde diese Schicht nur drei Millimeter dick sein. Aber obwohl Ozon nur in solch niedrigen Mengen vorkommt, ist es für das Leben auf der Erde von grundlegender Bedeutung. Denn das Ozon vermag zusammen mit dem gewöhnlichen Sauerstoff (O2) den größten Teil der ultravioletten Strahlung der Sonne zu absorbieren und verhindert dadurch, daß diese gefährliche Strahlung die Erdoberfläche erreicht. Ohne diese schützende Ozonschicht in der Atmosphäre könnten weder Tiere noch Pflanzen existieren, jedenfalls nicht auf dem Land. Es ist daher von größter Bedeutung, die Prozesse genau zu verstehen, die den Ozongehalt der Atmosphäre regeln.
Paul Crutzen, Mario Molina und Sherwood Rowland haben es durch ihre bahnbrechenden Leistungen ermöglicht, daß man heute die chemischen Prozesse der Bildung und des Abbaus von Ozon erklären kann. Ihr allerwichtigster Beitrag besteht darin, daß sie nachgewiesen haben, wie empfindlich die Ozonschicht auf die Emission gewisser durch die Menschheit verursachter Luftverunreinigungen reagiert. Es hat sich gezeigt, daß die dünne Ozonschicht eine Achillesferse der Menschheit darstellt, die durch scheinbar maßvolle Veränderungen der Zusammensetzung der Atmosphäre ernsthaft geschädigt werden kann. Durch ihre Klarlegung der chemischen Mechanismen, die die Konzentration des atmosphärischen Ozon bestimmen, wie durch ihre warnende Vorhersage vor den Folgen einer ungehemmten Emission ozonzerstörender Gase haben die drei Wissenschaftler dazu beigetragen, uns alle vor einem globalen Umweltproblem zu bewahren, das katastrophale Konsequenzen bekommen könnte.
Wie unser Wissen angewachsen ist
Ozon bildet sich in der Atmosphäre dadurch, daß gewöhnliche Sauerstoffmoleküle (O2) von der ultravioletten Strahlung der Sonne aufgespalten werden und daß die dabei freiwerdenden Sauerstoffatome mit molekularem Sauerstoff wie folgt reagieren:
O2 + UV-Licht =>2O
O + O2 + M =>O3 + M
wobei M ein beliebiges Luftmolekül (N2 oder O2) ist.
Der Engländer Sidney Chapman formulierte 1930 die erste photochemische Theorie für die Bildung wie auch für den Abbau des Ozons in der Atmosphäre. Diese Theorie, die beschreibt, wie sich die verschiedenen Erscheinungsformen des Sauerstoffs unter Einwirkung von Sonnenlicht ineinander umwandeln, vermochte zu erklären, warum die höchsten Gehalte an Ozon in einer Höhenschicht zwischen 15 und 50 Kilometern, der sogenannten Ozonschicht, vorkommen (Abb.1). Spätere Messungen ergaben jedoch beachtliche Abweichngen von Chapmans Theorie. Die berechneten Ozongehalte waren bedeutend höher als die beobachteten. Es mußte also andere chemische Reaktionen geben, die den Ozongehalt reduzierten. Der Belgier Marchel Nicolet trug später mit wichtigen Erkenntnissen bei, indem er zeigte, wie der Ozongehalt durch Reaktionen mit den durch chemische Zerlegung von Wasserdampf und Methan entstandenen Wasserstoffradikalen OH und HO2, beeinflußt wird.
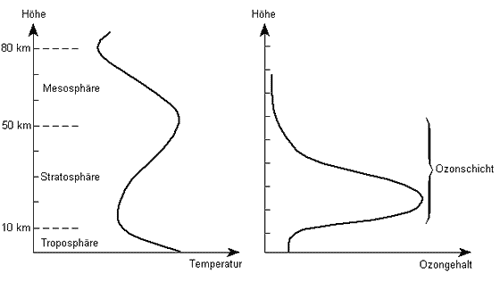 |
| Abb. 1. Temperatur und Ozongehalt auf dem Weg durch die Atmosphäre |
Paul Crutzen unternahm den nächsten grundsätzlichen Schritt zum Verständnis der Chemie der Ozonschicht. 1970 wies er nach, daß die Stickstoffoxide NO und NO2 katalytisch, ohne selbst verbraucht zu werden, mit Ozon reagieren und dadurch zu einer Verringerung des Ozongehalt beitragen.
NO + O3 => NO2 + O2
NO2 + O => NO + O2
O3 + UV-Licht =>O2 + O
________________________
Nettoergebnis: 2O3 => 3O2
Diese Stickstoffoxide entstehen in der Atmosphäre durch die Aufteilung des chemisch stabilen Stickstoffdioxides N2O, das stabiler ist und seinen Ursprung in mikrobiologischen Zersetzungsprozessen im Boden hat. Der Zusammenhang zwischen den Mikroorganismen im Boden und der Konzentration der Ozonschicht, den Crutzen nachgewiesen hat, wurde einer der Gründe, die zur schnellen Entwicklung der Forschung über den globalen biogeochemischen Kreislauf geführt haben.
Die zuerst wahrgenommene Bedrohung: Überschallflugzeuge
Die Fähigkeit der Stickstoffoxide, Ozon abzubauen, wurde bereits früh auch von dem amerikanischen Wissenschaftler Harold Johnston wahrgenommen, der in seinem Laboratorium umfassende Untersuchungen zur Chemie der Stickstoffverbindungen durchführte. Johnston wies 1971 darauf hin, dab die Ozonschicht durch die damals geplante Flotte von Überschallflugzeugen (SST-Flugzeuge; Super Sonic Traffic) bedroht sein könnte, da die bei hoher Temperatur arbeitenden Motoren dieser Flugzeuge besonders wirkungsvolle Quellen von Stickstoffoxiden sind, die auf 20 km Höhe direkt mitten in der Ozonschicht emittiert werden. Aufgrund der Arbeiten Johnstons und Crutzens begann in der Folgezeit eine sehr intensive Debatte zwischen Wissenschaftlern, Technikern, maßgeblichen Politikern und den zuständigen Behörden; sie standen auch am Anfang einer intensiven Forschung über die Chemie der Atmosphäre, die in den letzten Jahren große Fortschritte gemacht hat. (Daß die Pläne für eine große Flotte von Überschallflugzeugen aufgegeben wurden, beruhte nicht nur auf dem Umweltrisiko).
Spraydosen und Kühlschränke schaden der Ozonschicht
Der nächste große Fortschritt im Bereich der Ozonchemie wurde 1974 gemacht, als Mario Molina und Sherwood Rowland in der Zeitschrift Nature ihren Aufsehen erregenden Artikel über die Bedrohung der Ozonschicht durch Fluorchlorkohlenwasserstoffe (FCKW-Gase; Freone) veröffentlichten, die unter anderem als Treibgas in Spraydosen, als Kältemittel, beispielsweise in Kühlschränken, und bei der Herstellung von Schaumstoffen verwendet werden. Molina und Rowland konnten ihre Schlußfolgerungen mit zwei wichtigen Beiträgen anderer Wissenschaftler unterbauen:
– James Lovelock (England) hatte kurz zuvor eine verfeinerte Teknik entwickelt, um äuberst niedrige Gehalte organischer Gase in der Atmosphäre nachzuweisen (Elektroneneinfangdetektor). Mit Hilfe dieser Technik konnte Lovelock jetzt nachweisen, daß sich diese ausschließlich von Menschen erzeugten FCLW-Gase durch Bewegungen der Luft bereits in der gesamten Atmosphäre ausgebreitet hatten.
– Richard Stolarski und Ralph Cicerone (USA) hatten gezeigt, daß freie Chloratome in der Atmosphäre Ozon auf ähnliche Weise wie Stickstoffoxide katalytisch abbauen können.
Molina und Rowland sahen ein, daß die chemisch sehr stabilen FCKW-Gase so allmählich in die Ozonschicht der Stratosphäre transportiert und dort einem intensiven UV-Licht ausgesetzt werden. Dieses Sonnenlicht zersetzt auch die chemische gesehen sehr stabilen FCKW-Gase wobei freie Chloratome entstehen. Ihre Berechnungen ergaben, dab die Ozonschicht nach einigen Jahrzehnten um mehrere Prozent abnehmen würde, falls die Menschheit auch weiterhin in unverändertem Umfang FCKW-Gase verwendete. Diese Voraussage rief enorme Aufmerksamkeit hervor. FCKW-Gase waren bereits auf vielen technischen Gebieten verwendet worden, und man hielt sie im Hinblick auf die Umwelt aufgrund ihrer chemischen Stabilität und ihrer Freiheit von Giftwirkungen für geradezu ideal. Viele nahmen Molinas und Rowlands Berechnungen gegenüber einen sehr kritischen Standpunkt ein, doch die Gefahr einer verdünnten Ozonschicht beunruhigte noch mehr Leute. Heute wissen wir, daß sie in allem Wesentlichen Recht behalten haben. Es sollte sich sogar herausstellen, daß sie das Risiko unterschätzt hatten.
Das Ozonloch über der Antarktis
Molinas und Rowlands Bericht am Ende der 70er und Anfang der 80er Jahre hatte gewisse Begrenzungen der Emission von FCKW zur Folge. Aber erst 1985, als der wirkliche Schock kam, begannen ernsthafte internationalen Verhandlungen zur Frage der Emissionsbegrenzungen. Zu diesem Zeitpunkt hatten der Engländer Joseph Farman und seine Kollegen eine drastische und fortschreitende Abnahme der Ozonschicht über der Antarktis, die als das “Ozonloch” bekannt ist, entdeckt (Abb. 2). Zumindest zeitweise war die Verdünnung weitaus größer als in den vorhergegangenen Berechnungen der FCKW-Wirkung. Die Debatte zwischen den Wissenschaftlern wurde nun wesentlich intensiver geführt. Handelte es sich um eine natürlich bedingte Klimavariation oder um einen durch die Menschheit verursachten chemischen Abbau? Dank der bahnbrechenden Leistungen mehrerer Wissenschaftler, unter ihnen sowohl Crutzen, Molina und Rowland wie auch Susan Solomon und James Anderson, beide aus den USA, hat sich das Bild jetzt geklärt. Die Verdünnung wird in erster Linie auf die chemischen Reaktionen des Ozons auf Chlor und Brom industriell hergestellter Gase zurückgeführt.
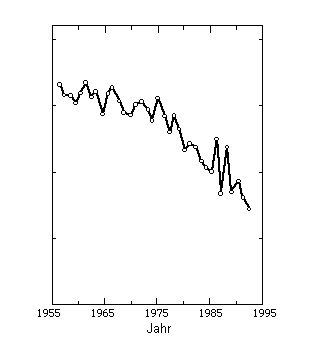
Abb. 2. Die Dicke der Ozonschicht (Durchschnittswerte im Monat Oktober) über der Halley-Bucht in der Antarktis. Man beachte die drastische Verdünnung seit Ende der 70er Jahre.
Die überraschend schnelle Reduktion des Ozongehaltes über der Antarktis läßt sich weder mit der Wirkung von Transporten noch mit konventionellen chemischen Reaktionen in der Gasphase erklären. Somit mußte es auch hier einen alternativen, den Abbau von Ozon beschleunigenden Mechanismus geben. Crutzen und andere identifizierten diesen Mechanismus als chemische Reaktionen auf der Oberfläche von Wolkenteilchen in der Stratosphäre. Daß gerade die Antarktis davon besonders betroffen wird, scheint mit den dort herrschenden extrem niedrigen Temperaturen zusammenzuhängen, die zur Kondensation von Wasser und Salpetersäure zu Stratosphären-Wolken im Polarbereich (“Polar Stratospheric Clouds”; PSCs) führen. Die Ozon abbauenden chemischen Reaktionen so u.a. die Freisetzung von katalytisch wirksamem Chlor, werden durch die Anwesenheit von Wolkenpartikeln effektiv gefördert. Diese Erkenntnis hat einen neuen, spannenden Zweig der Chemie der Atmosphäre ins Zentrum der Interesse gebracht: “heterogene” chemische Reaktionen auf Oberflächen fester Teilchen.
Die Ozonschicht und das Klima
Das Ozonproblem ist mit der interessanten Frage, wie die Menschheit das Klima beeinflußt, eng verbunden. Das dreiatomige Ozon ist, wie auch Kohlendioxid und Methan, ein Treibhaus-Gas das dazu beiträgt, die Temperatur auf der Erdoberfläche zu erhöhen (auch FCKW-Gase haben eine solche Wirkung). Modellberechnungen haben ergeben, daß das Klima besonders empfindlich auf Veränderungen des Ozongehalts in den unteren Luftlagern (Troposphäre) reagiert. Hier ist der Ozongehalt im letzten Jahrhundert vor allem durch die Emission von Stickstoffoxiden, Kohlenmonoxid und gasförmigen Kohlenstoffen, verursacht durch Kraftfahrzeuge und industrielle Prozesse sowie durch die Verbrennung von Biomasse in den Tropen, markant angestiegen. Der erhöhte Ozongehalt in den unteren Luftlagern ist aufgrund der Schäden, die dieser für Pflanzen und die menschliche Gesundheit zur Folge haben kann, ebenfalls ein Umweltproblem. Paul Crutzen ist führend unter den Wissenschaftlern in der Welt, die sich heute bemühen die chemischen Mechanismen darzulegen, die den Ozongehalt der untersten Atmosphärenschicht bestimmen.
Was können wir in Zukunft erwarten?
Dank der grundlegenden wissenschaftlichen Klärung des Ozonproblems – zum großen Teil das Verdienst der Arbeiten von Crutzen, Molina und Rowland! – konnte man weitgehende internationale Beschlüsse über ein Verbot der Emission ozonvernichtender Gase fassen. Ein Protokoll zum Schutz der Ozonschicht wurde unter der Regie der UNO ausgehandelt und 1987 in Montreal, Kanada, unterzeichnet. Die bisher letze Verschärfung des Protokolls von Montreal beinhaltet ein Totalverbot der gefährlichsten Gase ab 1996; den Entwicklungsländern wurden ein paar zusätzliche Jahre zugebilligt, um ozonfreundliche Ersatzstoffe einführen zu können. Da es eine gewisse Zeit dauert, bis die ozonvernichtenden Gase die Ozonschicht erreicht haben, müssen wir damit rechnen, dab die Abnahme der Ozonschicht sich noch einige weitere Jahre nicht nur über der Antarktis, sondern auch über Teilen der nördlichen Halbkugel ausweiten kann. Wenn die Verbote aber befolgt werden, sollte die Ozonschicht dennoch nach der Jahrhundertwende langsam zu heilen beginnen (Abb. 3). Es dürfte jedoch mindestens 100 Jahre dauern, bis sie völlig wiederhergestellt ist.
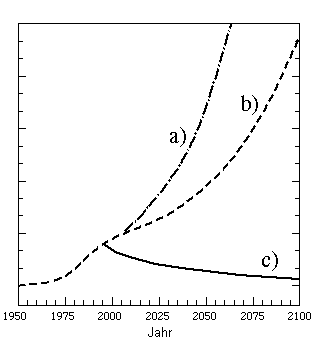 |
| Abb 3.Die bisherige Veränderung des Chlorgehalts in der Stratosphäre und drei verschiedene Szenarios für die Zukunft: a) Ohne Emissionsbegrenzung b) Begrenzungen gemäß des Protokolls von Montreal aus dem Jahre 1987 c) Die zur Zeit vereinbarten Emissionsbegrenzungen. Der Chlorgehalt als Maßstab der Größe der Ozonvernichtung. |
Lektürehinweise
Dotto, L. and Schiff, H. I., The ozone war, Doubleday, Garden City, New York, 1978.
Graedel, T. E. and Crutzen, P.J., Atmosphere, climate and change. Scientific American Library, 1995.
Gribbin, J., The hole in the sky, Corgi Books, London, 1988.
Rowland, F. S. and Molina, M. J., Ozone depletion: 20 years after the alarm, Chemical and Engineering News 72, 8-13, 1994.
Scientific assessment of ozone depletion 1994, WMO Report 37, World Meteorological Organization and United Nations Environment Programme, Geneva, 1995.
Toon, O. B. and Turco, R. P., Polar stratospheric clouds and ozone depletion, Scientific American 264, 68-74, 1991.
Wayne, R. P. Chemistry of Atmospheres, Oxford Science Publications, 1993.
WMO and the ozone issue, World Meteorological Organization, Report 778, 1992.
Paul Crutzen wurde 1933 in Amsterdam geboren. Niederländischer Staatsangehöriger. 1973 Doktor der Meteorologie an der Universität Stockholm. U.a. Mitglied der Königlich Schwedischen Akademie der Wissenschaften, der Königlich Schwedischen Akademie der Ingenieur-Wissenschaften, der Academia Europea.
Professor Paul Crutzen
Max-Planck-Institut für Chemie
Postfach 3060
D-55020 Mainz
Deutschland
Mario Molina wurde 1943 in Mexico City, Mexico geboren. PhD der physikalischen Chemie an der University of California, Berkeley. Mitglied der National Academy of Sciences der USA.
Professor Mario Molina
Department of Earth, Atmospheric and Planetary Sciences
MIT 54 – 1312
Cambridge, MA 02139
USA
F. Sherwood Rowland wurde 1927 in Delaware, Ohio, USA geboren. Doktor der Chemie an der University of Chicago. Mitglied der American Academy of Arts and Sciences und der US National Academy of Sciences, deren “Foreign Secretary” er zur Zeit ist.
Professor F. Sherwood Rowland
Department of Chemistry
University of California, Irvine, CA 92717
USA
Nobel Prizes and laureates
Six prizes were awarded for achievements that have conferred the greatest benefit to humankind. The 12 laureates' work and discoveries range from proteins' structures and machine learning to fighting for a world free of nuclear weapons.
See them all presented here.
